行業(yè)動(dòng)態(tài)
您當(dāng)前的位置 > 行業(yè)動(dòng)態(tài) > 行業(yè)法規(guī)
醫(yī)保局:藥企注意,9月30日前須完成這項(xiàng)工作...
加入日期:2019/6/29 10:20:33 查看人數(shù): 1206 作者:admin
6月27日,國(guó)家醫(yī)療保障局發(fā)布《關(guān)于印發(fā)醫(yī)療保障標(biāo)準(zhǔn)化工作指導(dǎo)意見(jiàn)的通知》(下稱《意見(jiàn)》)和《關(guān)于開(kāi)展醫(yī)保藥品、醫(yī)用耗材產(chǎn)品信息維護(hù)的通知》(下稱《通知》),旨在貫徹實(shí)施國(guó)家標(biāo)準(zhǔn)化戰(zhàn)略,加快形成全國(guó)統(tǒng)一的醫(yī)療保障標(biāo)準(zhǔn)化體系。
9月30日前完成產(chǎn)品信息維護(hù)
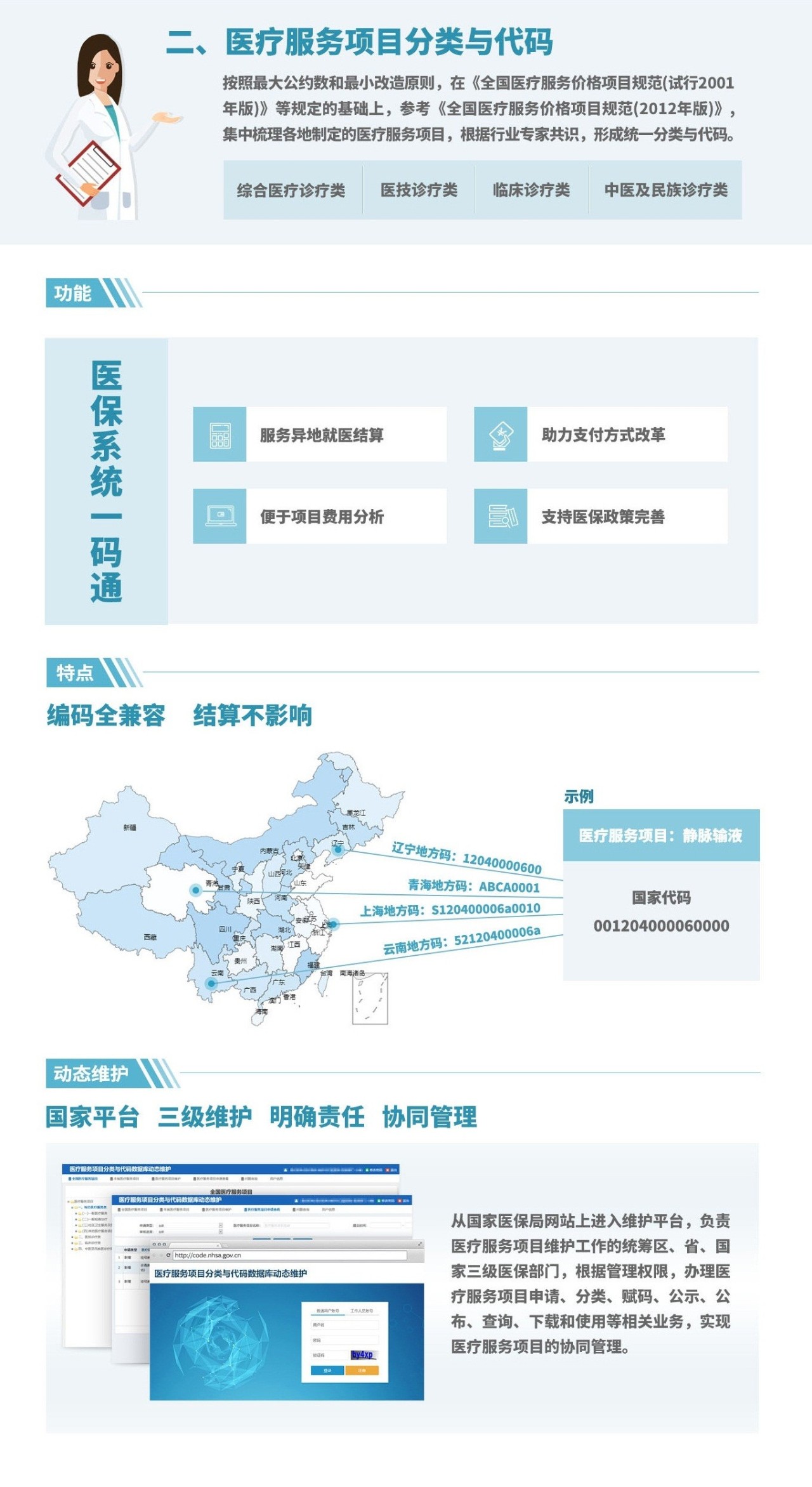
《意見(jiàn)》指出,將按照先試點(diǎn)完善、再推廣普及的方式,穩(wěn)妥推進(jìn)各類醫(yī)療保障標(biāo)準(zhǔn)的貫徹實(shí)施。前期重點(diǎn)開(kāi)展醫(yī)保疾病診斷和手術(shù)操作、醫(yī)療服務(wù)項(xiàng)目、藥品、醫(yī)用耗材4項(xiàng)信息業(yè)務(wù)編碼標(biāo)準(zhǔn)的測(cè)試使用,及時(shí)總結(jié)經(jīng)驗(yàn)做法,為其余11項(xiàng)信息業(yè)務(wù)編碼標(biāo)準(zhǔn)的全面實(shí)施提供可行經(jīng)驗(yàn)和示范引領(lǐng)。
與此同時(shí),醫(yī)保藥品、醫(yī)用耗材產(chǎn)品信息維護(hù)工作也開(kāi)始啟動(dòng)。根據(jù)《通知》,此次開(kāi)展的維護(hù)對(duì)象將包括藥品生產(chǎn)企業(yè)及進(jìn)口產(chǎn)品的國(guó)內(nèi)總代理、醫(yī)用耗材生產(chǎn)企業(yè)及進(jìn)口產(chǎn)品的國(guó)內(nèi)注冊(cè)代理人,維護(hù)品種覆蓋國(guó)家藥品監(jiān)督管理部門批準(zhǔn)上市的藥品和各級(jí)藥品監(jiān)督管理部門注冊(cè)、備案的單獨(dú)收費(fèi)醫(yī)用耗材。
各藥品、醫(yī)用耗材企業(yè)可以登錄國(guó)家醫(yī)療保障局官網(wǎng)(網(wǎng)址:www.nhsa.gov.cn),進(jìn)入“醫(yī)保業(yè)務(wù)編碼標(biāo)準(zhǔn)動(dòng)態(tài)維護(hù)”窗口,對(duì)產(chǎn)品信息進(jìn)行數(shù)據(jù)維護(hù)。企業(yè)提交的信息經(jīng)審核通過(guò)后將納入國(guó)家醫(yī)保信息業(yè)務(wù)編碼標(biāo)準(zhǔn)數(shù)據(jù)庫(kù),供各地醫(yī)療保障部門使用。
另一方面,《通知》對(duì)各藥企、醫(yī)用耗材企業(yè)的產(chǎn)品信息維護(hù)時(shí)限亦作出相應(yīng)要求:2019年6月30日(含)以前經(jīng)國(guó)家藥品監(jiān)督管理部門批準(zhǔn)上市的藥品和各級(jí)藥品監(jiān)督管理部門注冊(cè)、備案的單獨(dú)收費(fèi)醫(yī)用耗材,應(yīng)于2019年9月30日前完成相關(guān)產(chǎn)品信息維護(hù)工作。
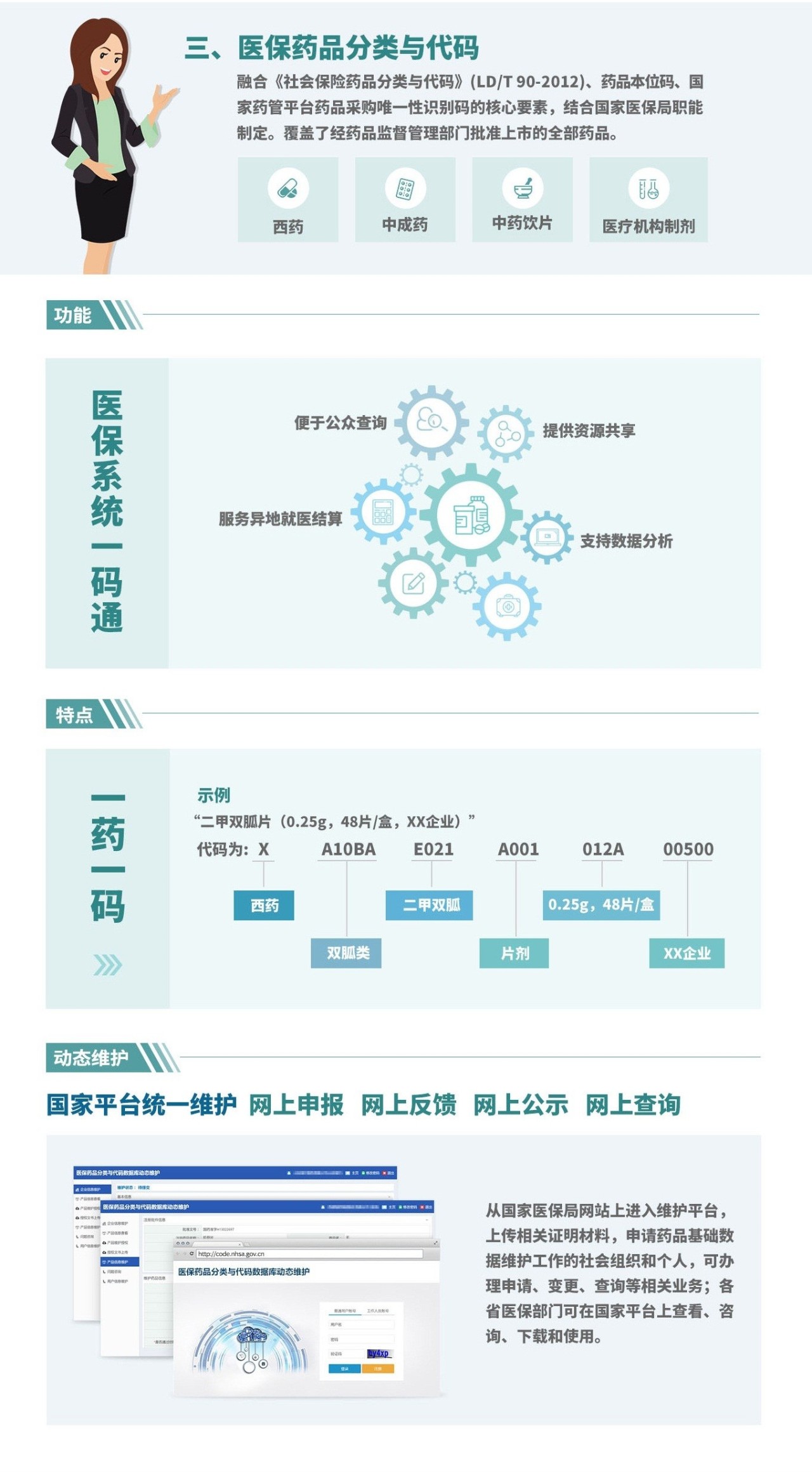
醫(yī)保藥品全新的編碼標(biāo)準(zhǔn)無(wú)疑最受產(chǎn)業(yè)關(guān)注。根據(jù)同日發(fā)布的《一圖讀懂:國(guó)家醫(yī)療保障信息業(yè)務(wù)編碼標(biāo)準(zhǔn)》,醫(yī)保藥品的分類與代碼融合了《社會(huì)保險(xiǎn)藥品分類與代碼》(LD/T 90-2012)、藥品本位碼、國(guó)家藥管平臺(tái)藥品采購(gòu)唯一性識(shí)別碼的核心要素,并結(jié)合國(guó)家醫(yī)保局職能制定,覆蓋了經(jīng)藥品監(jiān)督管理部門批準(zhǔn)上市的全部藥品?!耙凰幰淮a”的特征為藥品在全國(guó)“醫(yī)保系統(tǒng)一碼通”提供了可能,或?qū)?shí)現(xiàn)便于公眾查詢、提供資源共享、服務(wù)異地就醫(yī)結(jié)算、支持?jǐn)?shù)據(jù)分析等功能。
西藥與中成藥編碼規(guī)則
《意見(jiàn)》所帶附件公布了醫(yī)保疾病診斷和手術(shù)操作、醫(yī)療服務(wù)項(xiàng)目、藥品、醫(yī)用耗材4項(xiàng)信息業(yè)務(wù)編碼標(biāo)準(zhǔn),其中藥品項(xiàng)有西藥和中成藥的兩套編碼規(guī)則。
圖1 西藥編碼結(jié)構(gòu)
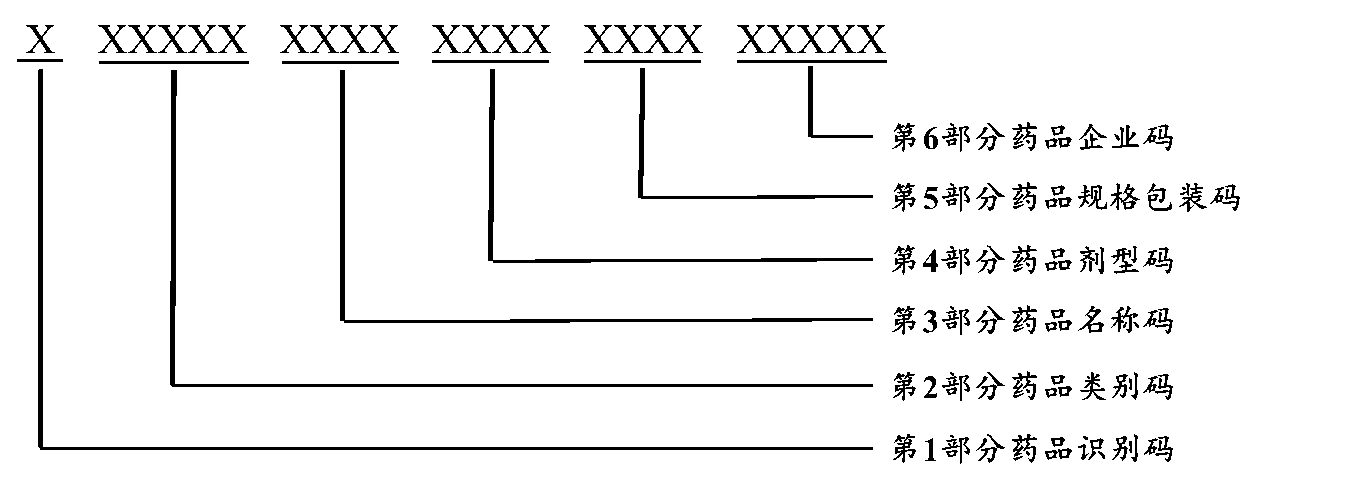
西藥編碼分6個(gè)部分共23位,通過(guò)大寫英文字母和阿拉伯?dāng)?shù)字按特定順序排列表示,其中:
第1部分是西藥藥品識(shí)別碼。用1位大寫英文字母“X”表示。
第2部分是西藥藥品類別碼。根據(jù)藥品活性物質(zhì)治療解剖系統(tǒng)、治療用途及藥理學(xué)作用劃分,分為4個(gè)層級(jí),共5位。第1層器官/解剖系統(tǒng)分類采用1位大寫英文字母表示,第2層藥理學(xué)/治療學(xué)分類采用2位阿拉伯?dāng)?shù)字表示,第3、4層化學(xué)/藥理學(xué)/治療學(xué)分類分別采用1位大寫英文字母表示。
第3部分是西藥藥品名稱碼。西藥藥品名稱采用中文通用名稱(不含劑型),原則上不包含命名中的鹽基、酸根部分。該碼由藥品名稱拼音首字母碼和藥品名稱碼兩部分組成,共4位。其中藥品名稱首字母碼用1位大寫英文字母表示,藥品名稱碼用3位阿拉伯?dāng)?shù)字表示。
第4部分是西藥藥品劑型碼。西藥藥品劑型除個(gè)別使用《國(guó)家基本醫(yī)療保險(xiǎn)、工傷保險(xiǎn)和生育保險(xiǎn)藥品目錄》(2017年版)中規(guī)定的劑型外,均為藥品注冊(cè)的劑型。該碼由劑型類別碼和藥品劑型碼2部分組成,共4位。其中劑型類別碼用1位大寫英文字母表示,藥品劑型碼用3位阿拉伯?dāng)?shù)字表示。
第5部分是西藥藥品規(guī)格包裝碼。藥品規(guī)格為藥品注冊(cè)批件的規(guī)格,藥品包裝為藥品補(bǔ)充申請(qǐng)批件的包裝。該碼由規(guī)格碼和包裝碼2部分組成,共4位。其中,規(guī)格碼用2位阿拉伯?dāng)?shù)字或大寫英文字母表示,包裝碼用2位阿拉伯?dāng)?shù)字或大寫英文字母表示。
第6部分是西藥藥品企業(yè)碼。藥品企業(yè)為藥品注冊(cè)批件的生產(chǎn)單位或公司名稱。西藥藥品企業(yè)碼為國(guó)家藥品監(jiān)督管理部門藥品本位碼中的5位藥品企業(yè)代碼。
圖2 中成藥編碼結(jié)構(gòu)

與西藥編碼類似,中成藥編碼亦分5個(gè)部分共20位,通過(guò)大寫英文字母和阿拉伯?dāng)?shù)字按特定順序排列表示,其中:
第1部分是中成藥藥品識(shí)別碼,用1位大寫英文字母“Z”表示。
第2部分是中成藥藥品類別碼。根據(jù)中成藥功能主治劃分,采用層次分類結(jié)構(gòu),分4個(gè)層級(jí),共5位。第1層功能主治采用1位大寫英文字母表示,第2層功能主治分類采用2位阿拉伯?dāng)?shù)字表示,第3層功能主治分類采用1位大寫英文字母表示,第4層功能主治分類采用1位大寫英文字母表示。
第3部分是中成藥藥品名稱碼。中成藥藥品名稱采用中文通用名稱(含劑型),該碼由藥品名稱首字母碼和藥品名稱碼2部分組成,共5位。藥品名稱首字母碼用1位大寫英文字母表示,藥品名稱碼用4位阿拉伯?dāng)?shù)字表示。由于中成藥藥品名稱中包含品種劑型,故不再對(duì)中成藥劑型另行賦碼。
第4部分是中成藥藥品規(guī)格包裝碼,藥品規(guī)格為藥品注冊(cè)批件的規(guī)格,藥品包裝為藥品補(bǔ)充申請(qǐng)批件的包裝。該碼由規(guī)格碼和包裝碼2部分組成,共4位。其中規(guī)格碼用2位阿拉伯?dāng)?shù)字或大寫英文字母表示,包裝碼用2位阿拉伯?dāng)?shù)字或大寫英文字母表示。
第5部分是中成藥藥品企業(yè)碼。藥品企業(yè)為藥品注冊(cè)批件的生產(chǎn)單位或公司名稱,該碼為國(guó)家藥品監(jiān)督管理部門藥品本位碼中的5位藥品企業(yè)代碼。